알코올 하면 쉽게 떠오르는 것이 술의 주요 성분인 에탄올인데 음주 후 체내에서 여러 과정을 통해 분해되어 최종적으로 이산화탄소와 물의 형태로 체외로 배출된다.
이런 분해과정에서 물이 많이 필요하므로 음주 후에는 갈증을 느끼게 된다. 또한 각 개인의 체질에 따라 체내 알코올 분해 능력에 차이가 있다. 반면, 메탄올은 체내에 분해효소가 없으므로 흡수 시 독성작용으로 인해 인체에 치명적인 악영향을 미치게 된다.

이러한 대사 과정을 통해 우리 몸은 알코올로부터 에너지를 흡수하여 필요할 때 사용하게 된다. 예를 들면 흡수된 에너지는 우리 몸의 기본 대사 과정에 사용하기도 하고, 몸을 움직이는데도 사용하고, 생각하거나 말을 하거나, 그 외에도 수 많은 활동에 사용하게 된다.
알코올이 가지고 있는 화학적 에너지는 그 외에도 여러 가지의 에너지 형태로 변신할 수 있다. 예를 들면 알코올을 태워서 나오는 열 에너지를 그대로 사용하여 요리를 하거나 방안을 따뜻하게 할 수도 있고, 화력 발전에서와 같이 그 열 에너지를 사용해 터빈을 돌려 전기를 발생시킬 수도 있고, 발생한 열 에너지나 전기를 장치를 움직이는 기계적 에너지로 변환시킬 수 도 있다.
이 중에서 전기를 발생시키는 방법을 한 번 다시 생각해 보자. 화력 발전에서처럼 열 에너지를 터빈을 돌리는 기계적 에너지로 변화시키는 과정에서 에너지의 많은 부분은 우리가 원하지 않는 것(예를 들면 주변 공기)의 온도를 높이는데 사용되어 낭비되고, 기계적 에너지를 전기 에너지로 변환시킬 때도 터빈이 돌면서 열이 나서 열 에너지로 일부 낭비되게 된다.
이러한 에너지 손실없이 알코올로부터 전기를 얻는 방법은 없을까? 현재까지 알려진 방법중에서 가장 근접한 답은 알코올 연료전지 일 것이다.
알코올 연료전지는 연료인 알코올을 연소시키지 않고 촉매를 사용한 화학 반응을 통해 전기를 발생시키는 장치이다. 직접 알코올을 연료전지에 주입해서 사용한다는 의미에서 '직접'이란 단어를 붙여 '직접 알코올 연료전지'라고 부르며 사용하는 알코올의 종류에 따라 직접 메탄올 연료전지, 직접 에탄올 연료전지 등으로 불린다.
'전기'라는 것은 간단히 표현하면 전자가 도선을 통해 흐르는 현상이다. 이렇게 볼 때 '어떻게 알코올로부터 전기를 만들어낼까?'라는 질문은 곧 ‘어떻게 알코올로부터 전자를 만들어 낼까'와 같은 물음이라는 것을 알 수 있다. 어떻게 핵과 전자로 구성된 원자가 여러 개 결합하여 분자를 이룬 알코올에서 전자를 떼어낼 수 있을까?
이것은 알코올을 태워서 물과 이산화탄소로 분해하는 것이 아니라, 촉매를 사용하여 물과 이산화탄소로 변화시키는 과정을 통해서 가능하며, 이것을 가능하도록 해주는 장치가 바로 알코올 연료전지이다.
기본적으로 연료전지는 양극에서 메탄올이 산화하여 생성된 전자(e-)와 양이온(H+)이 아래 그림에서와 같이 각각 외부도선과 전해질을 통해 산소 환원 반응이 일어나는 또 다른 하나의 전극표면으로 이동함으로써 전기를 생성하게 된다.
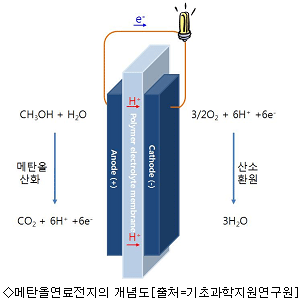
이때 각각의 전극표면에는 메탄올 산화 반응과 산소 환원 반응이 잘 일어날 수 있는 촉매(대표적인 예로 양극(anode)에는 PtRu, 음극(cathode)에는 Pt]가 있다. 양 전극 사이에는 전자는 통과하지 못하나 메탄올산화반응에서 생성된 H+이온이 양극에서 음극으로 통과할 수 있도록 하는 이온분리막 또는 전해질막이 있다. 이를 통해 전달된 H+이온은 음극에서의 산소환원반응에 참여하게 된다.
결과적으로 두 전극에서 각각 일어나는 메탄올 산화 반응과 산소 환원 반응이 합쳐져, 연료로 공급되는 메탄올이 이산화탄소와 물로 분해되는 과정 동안 외부도선에는 계속해서 전자의 흐름(전류)이 발생하게 되는 것이다.
연료전지의 일상생활에서의 폭넓은 이용을 위해서는 가격이 저렴하면서도 기능은 더 좋은 전지 소재 개발이 절실하다. 이런 이유로 메탄올연료전지와 관련해서 현재 진행되고 있는 많은 연구는 촉매활성이 뛰어난 촉매와 이온전도도가 높고 메탄올의 투과가 적은 분리막을 저렴하게 제작하는 기술을 개발하는데 집중되고 있다.
반면에 연료의 투과율이 상대적으로 심각하지 않으나 촉매에서 일어나는 연료의 산화 반응율이 떨어지는 에탄올연료전지에 대해서는 양극 촉매의 활성을 향상 시키는 기술 개발을 하는 것이 중요하다.
/한국기초과학지원연구원 대구센터 한옥희 분석연구부장, 한기성 박사

--comment--
첫 번째 댓글을 작성해 보세요.
댓글 바로가기